経頭蓋磁気刺激治療(TMS)とは? 保険外診療
TMS(Transcranial Magnetic Stimulation:経頭蓋磁気刺激)とは、コイルが生む磁気エネルギーを利用して、治療を受けられる患者さまは安静に座っているだけで、激しい痛みを伴うことなく、頭の皮膚の上から刺激するだけなので身体を傷つけることなく大脳や神経を刺激し、脳の特定部分を活性化する治療法です。
この治療を繰り返し行うことにより、脳の活動を引き起こし、現在まで多くの神経症状(頭痛、脳梗塞、パーキンソン症候群、ジストニア、耳鳴りなど)や精神医学的な症状(うつ病や幻聴など)に有効な治療法であることが報告されています。
当院でのTMSを受けるための条件
- 1.現在かかりつけである主治医の許可があり、自らの意思で治療を希望される方。
- 2.心臓ペースメーカーや人工内耳(補聴器)、インプラント、頭部にクリップ、コイル、ステント等の金属製医療機器が体内に埋め込まれていないこと。
- 3.うつ病の場合、継続的に薬剤を服用しているにもかかわらず、1年以上うつ症状が持続したり、再発を繰り返したり、薬剤による副作用が出ている方。
- 4.脳血管障害の場合、発症後1年以上経過していること。
- 5.慢性疼痛の場合、薬剤を服用しているにもかかわらず,6か月以上症状が持続している方。
- 6.重篤な身体の病気がなく、日常生活に介助を要しないこと。
- 7.20分以上の安静が保てること。
- 8.今までに痙攣の既往がないことを対象に行います。
※これらの基準を満たしていても担当医師の判断により、TMS治療を受けられないことがあります。
なお、TMSを受けるには医師の診察と許可が必要です。
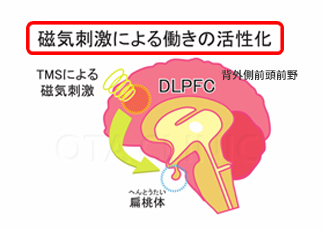
今までうつ病は“心の病気”と言われていましたが、最新の脳科学によって、実は“脳の病気”であると言われつつあります。これは、背外側前頭前野(DLPFC)という意欲や判断に関わる場所の活動が弱っている人がうつ病になると言われています。DLPFCが弱っていると扁桃体と呼ばれる恐怖や不安、悲しみといったネガティブな感情を出すところが暴走している状態になります。
TMSを繰り返し行うことによりDLPFCに磁気刺激を行い、低下している脳の活動を正常な状態に戻していくことによって意欲がわいて、かつ、脳の奥深くにある感情を司る部分である扁桃体を間接的に刺激することによって扁桃体の制御を取戻し、不安や悲しみが和らいできます。

この治療は麻酔などの必要がなく,治療中は覚醒した状態でリラックスしたまま治療を受けることができます。治療中に指で軽く叩かれるような軽い刺激があるだけで,抗うつ薬などにみられるような副作用はなく,安全性と優れた効果が特徴です。
また当院の機器は最新のモ-ドを搭載しているため、治療時間もより短くなっています(20~40分)。
この治療により、多くの方が、薬の減量あるいは薬を必要とせずに正常な生活に戻ることができます。
さらにこのTMSはうつ病だけではなく、認知機能の改善や脳こうそく後遺症、パーキンソン病、頭痛、不眠などにも効果が期待できると報告されています。
| 治療内容 | 目安の頻度 | 週に2~5回程度の治療(20回後に評価) |
|---|---|---|
| 検査 | 無し | |
| 費用 | 1回:16,100円(税込) | |
| TMS治療の適応症状 |
○ うつ病 ○ 双極性障害(躁うつ病) ○ 高いストレス状態 ○ 下記の症状とうつ病を併発している場合のうつ病治療 統合失調症/発達障害/適応障害/パーソナリティ障害/心身症/パニック障害/PTSD/依存症/身体表現性障害/PMS・PMDD/強迫性障害/認知機能の改善/脳梗塞後遺症/パーキンソン病/頭痛/不眠など |
|
| TMS治療が最適な人 とは |
○ うつ病がなかなか治らない ○ 抗うつ薬が効かない ○ 抗うつ薬の副作用がつらい ○ 抗うつ薬を減薬したい ○ 抗うつ薬の離脱症状が不安である ○ 抗うつ薬を服用することに抵抗がある ○ 身体への負担が少ない治療をしたい ○ 副作用が少ない治療をしたい ○ 電気けいれん療法はできれば受けたくない 磁気刺激治療(TMS)は、抗うつ薬による治療や電気けいれん療法で不安を感じている方に新たな選択肢になります。 |
|
| 副作用について | 軽度の頭痛程度/ごく稀にけいれん発(0.1%以下) ※ただし、治療中に少し頭部に刺激がある |
|
| 未承認医薬品等であることの明示、入手経路等の明示 | 本治療に用いる未承認医療機器は、医薬品医療機器等法上の承認を得ていないものですが、「医師等の個人輸入」により適法な輸入許可を得ています。日本では、未承認医療機器を、医師の責任において使用することができます。未承認医療機器についての情報「個人輸入において注意すべき医薬品等について」もご覧ください。 | |
| 国内の承認医薬品等の有無の明示 | 本治療に使用できる同一の性能を有する他の国内承認医療機器はありません。 | |
| 諸外国における安全性等 に係る情報の明示 |
韓国ではMFDS(食品医薬品安全省)の承認を2005年2月2日に取得、ヨーロッパではCEの承認を2014年6月13日に取得。 | |